Édition du génome
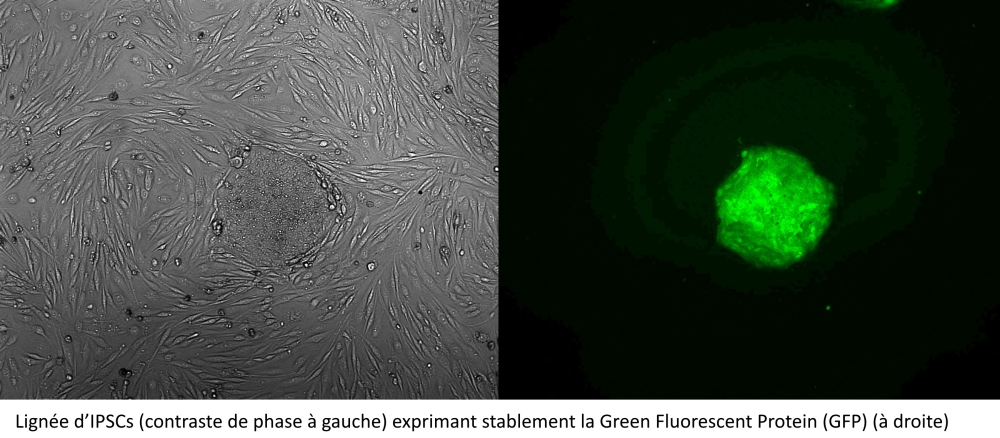
La plateforme d’Edition du Génome d’I-Stem est dédiée à la production de lignées de cellules souches pluripotentes humaines génétiquement modifiées pour l’étude et le traitement de maladies monogéniques à l’aide de la technologie CRISPR/Cas.
Contact : sbaghdoyan[AT]istem.fr
Depuis sa découverte, la technique d’édition de génome CRISPR-Cas9 ne cesse d’évoluer et d’offrir de nouvelles applications. Sur la plateforme, nous utilisons le système CRISPR-Cas (CASS) pour modifier le génome de lignées de cellules souches induites à la pluripotence (IPSCs) humaines par des approches de création d’indels (insertion/délétions de nucléotides), de Base Editing ou de recombinaison homologue (HDR, Homologous directed recombination).
Le but est de générer :
- des lignées d’IPSCs présentant une perte d’expression génique hétérozygote ou homozygote
- des lignées d’IPSCs « outils » pour suivre l’expression d’un gène ou induire sa surexpression
- des lignées d’IPSCs porteuses des mutations génétiques détectées chez un patient pour lequel on ne dispose pas de prélèvement cellulaire
- des lignées d’IPSCs isogéniques contrôles de lignées d’IPSCs de patients dans lesquelles la mutation génétique a été corrigée.
Les clones d’IPSCs génétiquement modifiés produits par la plateforme sont délivrés après des tests d’effet ON-TARGETS et OFF-TARGET du système CCAS et le contrôle de leur qualité (absence de mycoplasmes, maintien de la pluripotence et de l’intégrité génomique).
Équipe
Sandrine Baghdoyan, PhD-HDR
Resp. de Plateforme - IR INSERM
Pascal Fragner, PhD
Ingénieur Plateforme CECS
Publications
Generation and characterization of three human induced pluripotent stem cell lines from patients with glycogen storage disease type II.
01 octobre 2025
Stem cell research
Generation of three iPSC lines from patients with CACNA1S related congenital myopathy.
01 octobre 2025
Stem cell research
Semi-automated optimized method to isolate CRISPR/Cas9 edited human pluripotent stem cell clones.
27 avril 2023
Stem cell research & therapy
Équipement de l'équipe

Système d'électroporation Neon
Édition des lignées d’IPS.
Ce modèle est doté d’une chambre d’embout qui génère un champ électrique uniforme qui permet d’augmenter considérablement l’efficacité de la transfection et la viabilité des cellules.
CellCelector
Pour le clonage à haut débit des cellules éditées, nous utilisons cet automate de prélèvement de cellules individuelles et de colonies.

Bioanalyzer Agilent 2100
Pour l’évaluation de l’édition des clones, nous utilisons ce système d’électrophorèse automatisée.
FACS & CellInsigth CX7
Pour le contrôle du maintien de la pluripotence, la plasteforme CRISPR utilise un FACS (Miltenyi) ou le microscope automatisé CellInsigth CX7 (Cellomics ThermoFisher Scentific).