AUDIOWOLF
Étude d’efficacité de l’administration quotidienne de VPA (Valproate de sodium) ou DEPAKINE chez des patients atteints du syndrome de Wolfram.
Localisation :
2 sites :
- France: HEGP, Paris (PI: Dr Christophe Orssaud) – 11 patients déjà inclus et 5 patients traités.
- Espagne : UGC Almería Periferica (PI: Dr Gema Esteban Bueno) L’activation et l’ouverture du site sont plannifiés pour Avril 2023.
Résumé de l’étude :
Étude européenne de phase II, ouverte, non randomisée, avec assignation d’un seul groupe de 20 patients évaluables, âgés de plus de 13 ans , présentant une perte auditive neurosensorielle d’au moins 20 dB à 8 kHz en moyenne haute fréquence (HFA), ET présentant des mutations génétiques documentées dans le gène WFS1 ET présentant au moins un autre symptôme clinique majeur documenté relatif au syndrome de Wolfram (c.-à-d. diabète sucré, diabète insipide, atrophie optique). Tous les patients recevront pendant trois ans un traitement par VPA (Dépakine chrono).
NCT04940572 :
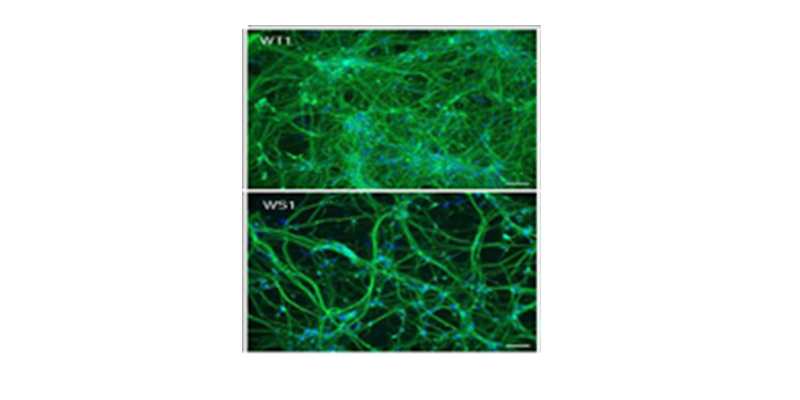
Neurones sains (WT) et neurones dérivés de cellules de patients atteints du syndrome de Wolfram (WS1).
La dose efficace et la durée de ce traitement de 3 ans doivent être déterminées individuellement dans le but d’obtenir une préservation de la fonction auditive définie par l’absence de diminution supérieure à 5 dB sur une oreille par rapport à la ligne de base à 8 kHz sur les hautes fréquences moyennes et de réduire la dose d’insuline et/ou de desmopressine nécessaire, c’est pourquoi la surveillance de la concentration plasmatique de VPA chez les patients est nécessaire pour l’ajustement de la dose.
En général, l’objectif est d’atteindre un taux plasmatique de valproate de sodium compris entre 40 et 100 mg/l (c’est-à-dire entre 300 et 700 micromol/l).
L’analyse comparera l’audiométrie tonale pure (PTA), l’indice d’interférence de la parole (SII) et le test auditif d’audiométrie tonale pure à haute fréquence entre la visite initiale et la visite finale.
- Date de début de l’étude : 26 novembre 2021
- Date d’achèvement primaire estimée : 1er novembre 2025
- Date prévue d’achèvement de l’étude : 1er décembre 2025
Dernière mise à jour :
11 patients inclus et 5 patients traités en France, le recrutement est actif.
En Espagne, le site commencera à recruter des patients en avril 2023. La soumission de l’essai clinique est en cours d’évaluation par l’autorité compétente locale.